נוסחה Osmolarity, כיצד לחשב את זה ואת ההבדל עם Osmolality
ה אוסמולריות הוא הפרמטר המודד את ריכוז התרכובת הכימית בליטר של תמיסה, כל עוד הוא תורם למאפיין הקוליגטיבי המכונה לחץ אוסמוטי של הפתרון.
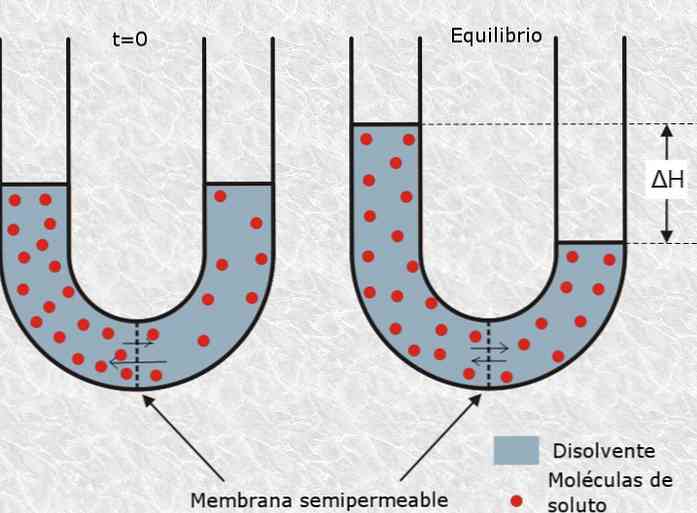
במובן זה, הלחץ האוסמוטי של פתרון מתייחס לכמות הלחץ הדרושה להאט את תהליך האוסמוזה, המוגדר כמעבר סלקטיבי של חלקיקים ממס באמצעות קרום חצי למחצה או נקבובי מתוך תמיסה של ריכוז נמוך יותר מרוכז.
כמו כן, היחידה המשמשת להביע את כמות החלקיקים המומסים היא Osmol (שסמל שלה הוא Osm), אשר אינו חלק ממערכת היחידות הבינלאומית (SI) המשמש כמעט את כל העולם. אז הריכוז של המומס בפתרון מוגדר ביחידות של Osmoles לליטר (Osm / l).
אינדקס
- 1 נוסחה
- 1.1 הגדרת המשתנים בנוסחת האוסמולריאציה
- כיצד לחשב את זה?
- 3 הבדלים בין osmolarity ו osmolality
- 4 הפניות
נוסחה
כאמור, osmolarity (הידוע גם בשם ריכוז אוסמוטי) באה לידי ביטוי ביחידות שהוגדרו Osm / l. זאת בשל הקשר שלה עם קביעת הלחץ האוסמוטי ואת המדידה של דיפוזיה ממס על ידי אוסמוזה.
בפועל, ריכוז אוסמוטי ניתן לקבוע כמות פיזית עם השימוש אוסמומטר.
האוסמומטר הוא מכשיר המשמש למדידת הלחץ האוסמוטי של פתרון, כמו גם קביעת תכונות קולגטיביות אחרות (כגון לחץ אדים, עליית נקודת רתיחה או דיכאון מקפיא) כדי להשיג את הערך של osmolarity של הפתרון.
בדרך זו, כדי לחשב את פרמטר המדידה, נעשה שימוש בנוסחה הבאה, אשר לוקחת בחשבון את כל הגורמים שעשויים להשפיע על תכונה זו..
Osmolarity = Σφiniגi
במשוואה זו, Osmolarity נקבעת כסכום הנובע מהכפלת כל הערכים המתקבלים משלושה פרמטרים שונים, אשר יוגדרו להלן.
הגדרת המשתנים בנוסחה האוסמוליטית
מלכתחילה הוא מקדם האוסמוטי, המיוצג על ידי האות היוונית φ (phi), אשר מסביר עד כמה הפתרון של ההתנהגות האידיאלית מתרחק, או במילים אחרות, את מידת אי-האידיאליות שהמוח מתבטא בפתרון.
בדרך הפשוטה ביותר, φ מתייחס למידת הדיסוציאציה של המומס, אשר יכול להיות בעל ערך בין אפס ואחד, כאשר הערך המרבי של היחידה מייצג ניתוק של 100%; כלומר, מוחלטת.
במקרים מסוימים - כמו סוכרוז - ערך זה עולה על אחדות; בעוד שבמקרים אחרים, כמו זו של מלחים, ההשפעה של אינטראקציות או כוחות אלקטרוסטטיים גורמת מקדם אוסמוטי עם ערך פחות מאחדות, גם אם מתרחשת דיסוציאציה מוחלטת.
מצד שני, הערך של n מציין את כמות החלקיקים שבהם ניתן לנתק את המולקולה. במקרה של מינים יוניים, נתרן כלורי (NaCl), אשר הערך של n שווה לשני, הוא נתון כדוגמה; ואילו במולקולת הגלוקוז הלא מיונן הערך של n שווה לאחת.
לבסוף, הערך של c מייצג את הריכוז של המומס, לידי ביטוי ביחידות טוחנת; ואת התמליל אני מתייחס לזהות של מומס מסוים, אבל זה חייב להיות זהה כאשר הכפלת שלושת הגורמים שהוזכרו לעיל ובכך קבלת osmolarity.
כיצד לחשב את זה?
במקרה של תרכובת יונית KBR (הידועה בשם אשלגן ברומיד), אם יש לך פתרון של ריכוז שווה 1 mol / l של KBR במים, זה מוסק כי יש לו osmolarity שווה 2 osmol / l.
זאת בשל אופי אלקטרוליט חזק שלה, אשר מעדיף disociation המלא שלה במים ומאפשר לשחרר שני יונים עצמאיים (K+ ואת בר-) שיש להם קצת חשמל, כך שכל שומה של KBR שווה שני osmoles בפתרון.
באופן אנלוגי, עבור פתרון עם ריכוז שווה 1 mol / l של BaCl2 (המכונה בריום כלור) במים, יש osmolarity שווה 3 osmol / l.
הסיבה לכך היא כי שלושה יונים עצמאיים משוחררים: יון Ba2+ ו שני יונים Cl-. לאחר מכן, כל שומה של BaCl2 הוא שווה לשלושה osmoles בפתרון.
מאידך גיסא, מינים שאינם יוניים אינם עוברים דיסוציאציה כזו ומקורם באוסמול יחיד עבור כל שומה של מומס. במקרה של תמיסת גלוקוז בריכוז שווה ל 1 mol / l, זה שווה 1 osmol / l של הפתרון.
הבדלים בין osmolarity ו osmolality
Osmol מוגדר כמספר החלקיקים כי הם מומסים בנפח שווה 22.4 l של ממס, נתון לטמפרטורה של 0 מעלות צלזיוס וגורמות לדור של לחץ אוסמוטי שווה 1 atm. יש לציין כי חלקיקים אלה נחשבים פעילים אוסמוטית.
במובן זה, המאפיינים הידועים בשם osmolarity ו osmolality מתייחסים לאותה מדידה: ריכוז המומס בתמיסה או, לשים בדרך אחרת, את התוכן של חלקיקים מוחלטים של תמיסה.
ההבדל הבסיסי שנוצר בין אוסמולריות ואוסמולציה הוא ביחידות שבהן כל אחד מיוצג:
Osmolarity מתבטא במונחים של כמות החומר לכל נפח של פתרון (כלומר, osmol / l), ואילו osmolality באה לידי ביטוי בכמות החומר לכל מסה של ממס (כלומר, osmol / ק"ג של פתרון).
בפועל, שני הפרמטרים משמשים באופן אדיש, אפילו מתבטאים ביחידות שונות, בשל העובדה כי קיים הבדל בלתי ניתן בין ההיקף הכולל של המדידות השונות.
הפניות
- ויקיפדיה. (s.f.). ריכוז אוסמוטי. מקור: es.wikipedia.org
- Chang, R. (2007). כימיה, מהדורה תשיעית. מקסיקו: מקגרו-היל.
- אוונס, ד 'ח' (2008). תקנה אוסמוטית ויונית: תאים ובעלי חיים. מאוחזר מ- books.google.co.il
- פוטס, W. T, ו פארי, W. (2016). תקנה אוסמוטית ויונית בבעלי חיים. מאוחזר מ- books.google.co.il
- ארמיטג ', ק (2012). חקירות ביולוגיה כללית. מאוחזר מ- books.google.co.il


