מחלת פאהר תסמינים, גורמים, טיפול
ה מחלת פאהר היא מחלה גנטית תורשתית קשורה בהתפתחות של הסתיידויות מוחין (פולו Verbel, טורס זמבראנו, Cabarcas ברבוסה, נאבאס גונזלס, מונטויה ואת Bolaños גרסיה, 2011).
הפרעה זו מאופיינת בעיקר על ידי נוכחות של הפרעות נוירולוגיות פסיכיאטריות. חלקן קשורות להידרדרות תפקודים מנטליים, שינויים מוטוריים או הפרעות התנהגותיות (Polo Verber et al, 2011).
גורמים ספציפיים של מחלה אינם ידועים במדויק (פרז ואח '., 2012). מחברים אחדים כמו אוביידו גמבואה ו Santiesteban זגארה (2012), מתייחסים האטיולוגיה עם עיוות גנטי הממוקם על כרומוזום 14. זה מייצר הסתיידות הבילטרליים ומתקדמת של אזורים שונים במוח, בעיקר בגרעיני הבסיס ואת קליפת המוח (אוביידו גמבואה זגארה ו Santiesteban, 2012).
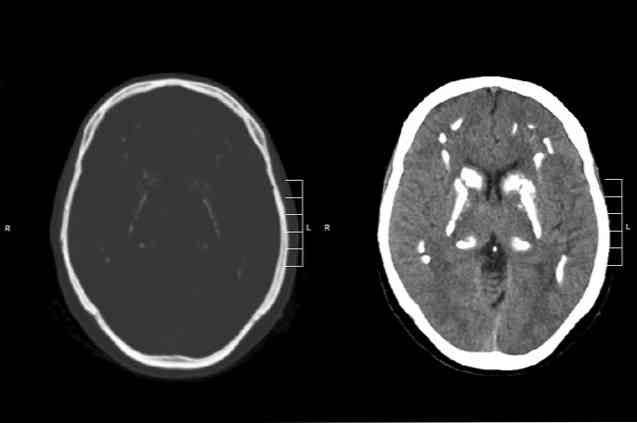
האבחנה של הפרעה נוירודגנרטיבית זו מבוססת בעיקר על השימוש בבדיקות הדמייה (Pérez Maciá, Martínez Cortés, Pecino Esquerdo, García Fernández, 2012).
בדרך כלל, הטכניקה של בחירה היא ממוחשבת טומוגרפיה צירית ללא ניגודיות (Pérez Maciá et al, 2012).
אין תרופה לתסמונת Fahr, וגם אין טיפול ספציפי (Lacoma Latre, Sánchez Lalana, Rubio Barlés, 2016).
בדרך כלל נעשה שימוש בגישה רפואית סימפטומטית ושיקומית. עם זאת, הפרוגנוזה של אנשים הסובלים מתסמונת Fahr היא שלילית (Oviedo Gamboa ו Zegarra Santiesteban, 2012).
זוהי מחלה שמייצרת פגיעה מתמשכת ומעכבת (Oviedo Gamboa ו- Zegarra Santiesteban, 2012).
מאפיינים של מחלת פאהר
מחלת פאהר היא הפרעה ממוצא גנטי דומיננטי, המאופיינת על ידי נוכחות של הפרעות נוירולוגיות ופסיכיאטריות (המכון הלאומי להפרעות נוירולוגיות ושבץ, 2016).
זוהי הפרעה נוירולוגית ניוונית שתגרום להידרדרות שיטתית של יכולות קוגניטיביות, מיומנויות מוטוריות או התנהגות. בנוסף, זה יכול להיות מלווה סיבוכים אחרים כגון פרקים עווית (הארגון הלאומי להפרעות נדירות, 2016).
בספרות הרפואית בדרך כלל הם משתמשים במגוון של תנאי להתייחס להפרעה זו: הסתיידות מוחין המשפחה העיקרית, ferrocalcinosis מוחין, תסמונת פאחר, ferrocalcinosis cerbro כלי הדם, הסתיידות מוחין אידיופטית, וכו ' (הארגון הלאומי להפרעות נדירות, 2016).
התסמונת Fahr מונח המשמש לעתים קרובות בקושי להגדיר תמונה קלינית האטיולוגיה אשר אינו מוגדר בבירור או הקשורים הפרעות מטבוליות או אופי אוטואימוניות (אוביידו גמבואה ו זגארה Santiesteban, 2012).
מצבו של פאהר, המונח "פאהר", מתייחס להפרעה הנגרמת למקור גנטי תורשתי (Oviedo Gamboa ו- Zegarra Santiesteban, 2012).
בשני המקרים, הסימנים והתסמינים קשורים עם נוכחות של calcifications באזורים שונים במוח..
חשיבות הסידן
סידן הוא מרכיב ביוכימיים מפתח הגוף שלנו. תפקידיה מכסים מגוון רחב של רגולצית השפעת קצב לב, ייצור הורמון, לשלוט קרישת דם, ויסות של פעילות שרירים או פעילות המוח (National Institutes of Health, 2015).
הגוף שלנו מורכב כמות גדולה של סידן, כ 1000 גרם אנשים של בגרות (Gummez Giraldo, 2016). בנוסף, יש לנו מגוון רחב של מנגנונים המאפשרים לנו לשלוט על נפח והפצה שלהם (האגודה האמריקאית של אונקולוגיה קלינית, 2016).
גורמים פתולוגיים שונים כגון אנומליות גנטיות יכולים לשנות את שיווי המשקל שלהם המוביל היפרקלצמיה, הסתיידות של מבנים, וכו '.
עם המושג הסתיידות אנו מתייחסים לתהליך חריג המייצר הצטברות פתולוגית של סידן בכל מבנה של האורגניזם שלנו.
במקרה של המוח, מוגדר על ידי ההצטברות של סידן בתוך כלי דם בעורקי ורידים הקטנים, בנוסף הנימים (Pamo-ריינה, Cumpa-Quiroz, רוסאלס-מנדוזה, שיער Gavidia, 2016).
מצב זה יפיק שינוי של זרימת הדם ופציעות רקמות עצביות, בין מחלות אחרות. כל אלה אחראים על התפתחות סימפטומטולוגיה של תסמונת Fahr.
בדרך כלל זה משפיע על אזורים קליפת המוח ו subcortical (פאמו-ריינה, Cumpa-Quiroz, Rosales-Mendoza, Cabellos-Gavidia, 2016).
האזורים הפגועים ביותר הם הגרעינים הבסיסיים או הגרעינים הבסיסיים. מבנה מוח זה ממלא תפקיד חיוני ברגולציה ובתחילת התנועה (Neurowikia, 2016).
במקרים מסוימים ניתן למצוא גם פקד לא תקין של ברזל, אלומיניום, אבץ או מגנזיום (Pamo-Reyna et al, 2016).
המנגנון הספציפי שבו הצטברות של חומר זה מתרחשת עדיין לא ידוע. כמה מחברים, כגון אוביידו Gamboa ו Zegarra Sanesteban (2012), מציע כמה השערות:
- ריכוז סידן חריג ברמה הפנים תאית נוספת.
- ריכוזי פוספט חריגים.
- חריגות במחסום הדם במוח.
- הפחתת זרימת הדם באזורי מוח שונים.
בשנת 1850 החלו לזהות אנומליות נוירולוגיות שונות הקשורות לתסמונת פאהר (Polo Verber et al, 2011).
זה היה Delacour אשר תיאר את נוכחותם של calcifications כלי הדם באזורים של הגרעינים הבסיסיים הקשורים בסימפטומים נוירולוגיים בחולה בן 56 (פולו Verber et al, 2011).
בשנים שלאחר מכן, חוקרים אחרים, כגון במברגר, תיארו ממצאים קליניים באמצעות ניתוח היסטופתולוגי של הסתיידות מוחית (Polo Verber et al, 2011).
זה התייחס לנוכחות של הסתיידות בכלי הדם הקטנים במוח הקשורים להיסטוריה רפואית של פרקים אפילפטיים ונכות אינטלקטואלית (Polo Verber et al, 2011).
זה לא היה עד 1930 כאשר תיאודור פאר התייחס לתמונה הרפואית הזאת כאל גוף קליני עצמאי, המתואר כחולי פאהר (פאמו-ריינה ואח ', 2016).
האם זה פתולוגיה תכופה?
מחלת פאהר היא הפרעה נוירולוגית נדירה באוכלוסייה הכללית (סלים ואחרים, 2013). בדרך כלל מסווגים כמו מחלות נדירות.
הניתוח האפידמיולוגי מקשר את שכיחותו למקרה אחד לפחות למיליון איש ברחבי העולם (סלים ואח ', 2013).
בדרך כלל, שכיחותו נוטה לעלות עם הגיל (Carrillo, Álvarez de Sotomayor, לוצנה, קסטרו ו Izquierdo, 2006).
התחלתה האופיינית של מחלה זו נופלת בין העשור השלישי לחמישי של החיים (Cassiani et al., 2015).
בנוסף, זוהו שני פסגות של שכיחות מקסימלית (Pérez Maciá et al., 2012):
- תחילת הבמה הבוגרת: יש סימפטומטולוגיה המאופיינת בשינויים פסיכיאטריים.
- מ 50-60 שנים של גיל: e מציג סימפטומטולוגיה המאופיינת בהידרדרות קוגניטיבית ושינויים פסיכו-מוטוריים. תסמינים פסיכיאטריים, במיוחד שינויים רגשיים, נמצאים גם בשלב זה.
סימנים ותסמינים
מחלת פאהר מוגדרת ביסודה על ידי נוכחות ופיתוח של הפרעות נוירולוגיות ופסיכיאטריות (Saleem et al., 2013).
הבא, נתאר כמה מן הנפוצים ביותר:
שינויים נוירולוגיים
- היפו / שריר היפרטוניה: טון שרירים משתנה ברוב המקרים. ייתכן שיש רפיון משמעותי או נוקשות. תנועות וולונטריות ולא רצוניות מופחתות לעתים קרובות.
- רעד: אנו יכולים לזהות את הנוכחות של תנועה רצונית קבועה לא רצונית. זה בדרך כלל משפיע על הראש, הידיים והידיים.
- פרקינסון: ייתכן כי הרעידות וסימפטומים אחרים מתפתחים לקראת תמונה קלינית הדומה לזו של פרקינסון. התכונות הנפוצות ביותר הן רעד של מנוחה, היעדר תנועה מרצון, קשיחות שרירים, אי יציבות יציבה וכו '..
- שיתוק ספסטי: קבוצות השרירים השונות משיגות טונוס שרירים גבוה מאוד המונע מימוש של כל סוג של תנועה. זה סוג של שיתוק יכול להוביל להתפתחות monoparesis / monoplegia, hemiparesis / hemiplegia, diparesia / diplegia, tetraparesis / tetrapegia.
- שיתוק אתיופי: טונוס השרירים נוטה להשתנות בהתמדה, מה שמוביל להתפתחות של תנועות לא רצוניות ו / או רפלקסים פרימיטיביים.
- אפראקסיות מוטוריות: נוכחות של קושי ניכר או חוסר יכולת לבצע פעולות מוטוריות הקשורות לתהליך תכנון קודם (רצפים, מטרות / יעדים, הדרכה וכו ')..
- התקפים עוויתיים: התפתחות של פרקים של התכווצויות שרירים התכווצויות או תסיסה מוטורית הקשורים בפעילות נוירונים חריגה סינכרוני הוא תכופות. פרקים של אובדן זמני של תודעה או תפיסה של תחושות תפיסתי חריגות (גירויים אור, עקצוץ, וכו ') עשוי להופיע גם..
- גירעון קוגניטיבי: המאפיין האופייני ביותר של חולים המושפעים מתסמונת פאהר הוא ההידרדרות המתקדמת של היכולות המנטליות. הנפוץ ביותר הוא לבחון מחויבות קשב, הפחתת מהירות העיבוד, דיסאוריינטציה במרחב-זמן או בעיות בזיכרון. בדרך כלל, התיבה הזו מכונה תהליך פסאודו-מטורף.
- הפרעות שפה: מטופלים מתחילים בקושי לשמור על חוט השיחה, למצוא את המילים הנכונות או לבטא את השפה. סוג זה של אנומליות יכול להתקדם לקראת בידוד חלקי או מוחלט של תקשורת.
הפרעות פסיכיאטריות
- הפרעות התנהגותיות: דפוסים של התנהגויות משתנות מופיעים בדרך כלל. אלה מאופיינים בעיקר על ידי נוכחות של פעילויות חוזרות ונשנות התנהגויות סטריאוטיפיות. אנשים מושפעים נוטים לבצע את אותו סוג של פעילות בהתמדה. בנוסף, הם מציגים התנהגות לא ברורה או לא הולמת למצבים הקשריים.
- שינויים אישיותיים: התכונות האישיות של האדם המושפע מסולפות לעיתים קרובות ומביאות לרגשות רגשית, עצבנות, חוסר יוזמה, הסרת הדמיון, בידוד חברתי, חרדה.
- פסיכוזה: יש איבוד משמעותי במגע עם המציאות. אובססיות, אמונות שווא, אשליות או הזיות נראות בדרך כלל.
- משבר הסערות: פרקים של תוקפנות, תסיסה מוטורית, חוסר מנוחה, עצבנות, דיבור לא מאורגן או אופוריה עשויים להתפתח.
- דיכאון: אפשר קצת יותר או תסמינים הקשורים בהפרעת דיכאון וחוסר תקווה, עצבות, עצבנות, איבוד עניין, עייפות מתמדת, קשיי ריכוז, הפרעות שינה, מחשבות על מוות, כאב ראש להופיע, וכו '.
סיבות
סופרים כמו Lacoma Latre, סאנצ'ס Lalana ו רוביו ברלס (2016) מגדירים מחלת Fahr כמו תסמונת האטיולוגיה לא צוינה או לא ידוע קשורה להתפתחות של הסתיידויות הבילטרליים באזורי מוח שונים.
עם זאת, אחר כמו Cassani-מירנדה, Herazo-בוסטוס, קבררה-גונזלס, שרשרת-ראמוס ו באריוס Ayola (2015) להתייחס ארנבות גנטיות תורשתיות ללא שכיחות גורמים רעילים זיהומיות, טראומתיים, אחרים, ביוכימית או מערכתית.
מקורו קשור שינוי גנטי המקומי על כרומוזום 14 (אוביידו גמבואה ו זגארה Santiesteban, 2012) ואת גן SLC20A2 המשויך (Reference בית הגנטיקה, 2016).
גן זה אחראי בעיקר על מתן הוראות ביוכימיות לייצור סוג של חלבון. יש לו תפקיד חיוני רגולציה אורגנית של רמות פוספט, בין פונקציות אחרות (גנטיקה דף הבית הפניה, 2016).
כמה מחקרים קליניים, כמו זה של וואנג ועמיתיו (2012), קשרו את המוטציות בגן SLC20A2 ואת הקורס הקליני של תסמונת Fahr במספר משפחות (הארגון הלאומי להפרעות נדירות, 2016)..
בנוסף, זוהה סוג אחר של אנומליות גנטיות הקשורות לתסמונת Fahr: מוטציות בגן PDGF ו- PDGFRB (הארגון הלאומי להפרעות נדירות, 2016).
אבחון
האבחנה של מחלת פאהר דורשת שילוב של בדיקה נוירולוגית ופסיכיאטרית.
במקרה של בדיקה נוירולוגית, ההתערבות הבסיסית מבוססת על ביצוע של טומוגרפיה ממוחשבת (Pérez Maciá et al, 2012).
סוג זה של טכניקת הדמייה מאפשר לנו לזהות את הנוכחות ואת המיקום של calcifications מוחין (Pérez Maciá et al., 2012).
חיוני לבצע הערכה נוירופסיכולוגית כדי לציין את כל הספקטרום של הפרעות קוגניטיביות ופסיכומוטוריות וחריגות.
סוג של בדיקות neuropsychological כי ניתן להשתמש הוא רחב, בדרך כלל תלוי בבחירה של מקצועי. חלק מהשימוש הנפוץ ביותר הוא: סולם המודיעין של Wechler למבוגרים (WAIS), השלמת דמות המלך, בדיקת Stroop, בדיקת TMT Trace וכד '. (Cassani-Miranda et al., 2015).
בנוסף, כל הערכה זו מלווה בהערכה פסיכולוגית ופסיכיאטרית לזיהוי שינויים הקשורים במצב הרוח, תפיסת המציאות, דפוסי ההתנהגות וכד '..
טיפול
כפי שציינו בתיאור הראשוני, עדיין אין תרופה לתסמונת פאהר (לאקומה לאטר, סאנצ'ס ללנה, רוביו ברלס, 2016).
בסיסי התערבויות רפואיות מופנות כלפי סימפטומים בטיפול וסיבוכים רפואיים: תרופה לטיפול בהתקפים, קוגניטיביים שיקום המידרדר יכולת מנטלית או שיקום פיזי של סיבוכים מוטוריים.
למרות שיש טיפולים ניסיוניים, הם בדרך כלל לא מדווחים על יתרונות משמעותיים.
מהי התחזית הרפואית של האנשים המושפעים?
ליקוי קוגניטיבי, פיזי ופונקציונאלי הוא מעריכי. מחלה זו בדרך כלל מתקדמת לקראת תלות מוחלטת ואת המוות הבלתי נמנע של האדם המושפע.
הפניות
- ADCO. (2016). היפרקלצמיה. מתוך האגודה האמריקנית לאונקולוגיה קלינית.
- Carrillo, R., Álvarez de Sotomayor, J., Lucena, C., Castro, D., & Izquierdo, G. (2006). מחלת פאהר והיריון. הקליני.
- Cossani-Miranda, C., Herazo-Bustos, M., Cabrera-Gonzalez, A., Cadena-Ramos, I., & Barrios-Ayola, F. (2015). פסיכוזה הקשורה לתסמונת פאהר: דו"ח מקרה. קולום.
- Gummez Giraldo, C. (2016). היפרקלצמיה והיפוקלצמיה.
- Lacoma Latre, E., Sánchez Lalana, E., & Rubio Barlés, P. (2016). מחלת פאהר. תמונה אבחון.
- NIH. (2016). תסמונת פאהר. מקור: המכון הלאומי להפרעות נוירולוגיות ושבץ.
- NIH. (2016). SLC20A2. מקורו של דף הבית של גנטיקה.
- NORD (2016). ראשוני ראשוני מוחי Calcification. נלקח מן הארגון הלאומי להפרעות נדירות.
- Oviedo Gamboa, I., & Zegarra Santiesteban, W. (2012). מאפיינים טומוגרפיים בחולה עם תסמונת פאהר, ביחס למקרה. Gac Med קערה.
- פאמו-רינה, א ', קאמפה-קירוז, ר', רוזאלס-מנדוזה, ק ', & Cabelos-Gavidia, ד' (2016). מחלת פאהר. תמונה קלינית.
- Pérez Maciá, V., Martínez Cortés, M., Pecino Esquerdo, B., & García Fernández, L. (2012). מצגת לא טיפוסית של תסמינים פסיכיאטריים: מחלת פאהר. Psiq Biol.
- פולו Verbel, L., סאמברנו טורס, M., Cabarcas Borbosa, O., נאבאס, ג, גונזלס, א מונטויה, M., & Bolanos גרסיה, ר '(2011). פאחר המחלה גורם נדיר של הסתיידויות מוחין. אקטה נירול קולומבוס /.
- סלים ואח ',. (2013). תסמונת פאהר: סקירת ספרות של עדויות עדכניות. כתב העת Orphanet של מחלות נדירות.


