מנגן אוקסיד (MnO2) מבנה כימי, תכונות ושימושים
ה תחמוצת מנגן (MnO)2) הוא תרכובת כימית אנאורגנית שנוצרו על ידי האלמנט מנגן עם מספר חמצון +4 וחמצן, אשר במבנה של תחמוצות יש מספר חמצון של -2. זה ידוע גם על ידי שמות של מנגן (IV) תחמוצת אנהידריד מנגן.
הוא מוצק מן הקפה שחור כהה. זה בטבע כמו פירולוסיט מינרליים, שחור מגובש להרכיב דנדריטים (הארכות מסועפות). זה ניתן להשיג כמו שאריות שחור התגובה בין אתילן אשלגן permanganate לאחר היווצרות של גליקול על ידי פעילות חמצון של permanganate אשלגן.

חשוב מאוד בתעשיית הזכוכית בשל אופיו של סוכן חמצון, שכן הוא מבטל את הצבע הירוק מגיע תרכובות ברזלי וממיר אותם לתוך ברזלי.
אינדקס
- מבנה כימי
- 2 מאפיינים
- 3 שימושים
- 3.1 כזרז
- השפעות על הבריאות
- 5 הפניות
מבנה כימי
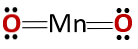
המבנה הכימי של המתחם מתאים לזה של אנהידריד ולא לזה של תחמוצת בסיסית, כפי שצפוי כי הוא מורכב ממתכת ולא מתכת.
מקרה מיוחד זה נובע מן ההתנהגות שהניח מנגן במצבי החמצון השונים שיש לו. לפיכך, עבור מדינות החימצון +2 ו -3 צורות תחמוצות MnO ו Mn2הו3 בהתאמה, כי כאשר מגיבים עם מים הם יוצרים את hydroxide מנגן ו hydroxide מנגן, בהתאמה.
עם זאת, Mn2הו3 במדיום חומצי מעט הוא מתנהג כמו אנהידריד. עם מצבי החימצון +4, +6 ו +7, MnO2, את MNO3 ואת MnO4 הם יוצרים חומצות כאשר מגיבים עם מים.
במדיום קצת חומצי MnO2 זה מתנהג כמו תחמוצת בסיסית, כך שזה יכול ליצור hydroxide המקביל.
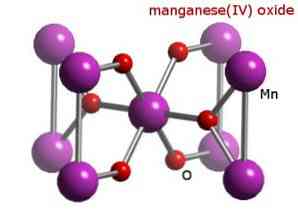

יש לזכור כי במקרה זה אין אזכור של תכונות amphoteric, לפיו מתחם יכול להתנהג כמו חומצה או כבסיס. זהו מקרה מיוחד של התנהגות Mn.
מאפיינים
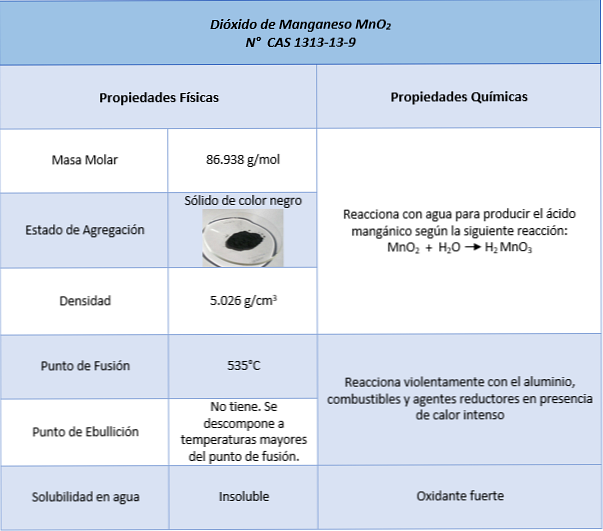
שימושים
- הוא משמש כמקור של מנגן
- כמו חמצון סוללות אלקליין
- צבעי זכוכית, קרמיקה וחרסינה.
- בהשגת כלור ויוד.
- ב פירוק של מי חמצן להיווצרות של חמצן גז ומים.
- בתגובת הפירוק של chlorate אשלגן לייצור של חמצן גז אשלגן כלוריד.
- ממיסים באצטון או ב dichloromethane, מחמצן את האלכוהול העיקרי לאלדהידים ומשניים לקטונים.
- תעשיית סוללות אלקליות.
כזרז
זה חל על תגובות הפחתת תחמוצת, להסרת גופרתי כגון H2S ו קטיונים כמו Fe+2 ו Mn+2 , ארסן ורדיו שנמצאו במי התהום המזוהמים על ידי סוג זה של תרכובות.
זיהום זה עלול להיוצר, אם לא מבוקר השלכת חומרים רעילים, על ידי שטיפה של קרקע מזוהמת או על ידי הנוכחות של יסודות כימיים בזמן השאיבה.
MNO2 טוהר גבוהה המתקבל pyrolusite המשמש מסנן (פילוקס) היא האמצעי היעיל ביותר כדי להסיר את זה סוג של זיהומים ממי תהום.
השפעות על הבריאות
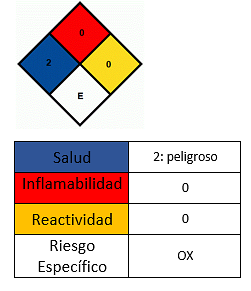
- הימנע ממגע עם העור.
- במקרה של מגע, שטפו את האזור המתאים.
- לא שואפים את האבקות.
- גירוי ואדמומיות ניתן לראות במגע עין. לשטוף עם הרבה מים, לתת למים לרוץ דרך העיניים ולקרוא לעזרה רפואית במקרה של רציני.
- במגע עם גירוי העור אדמומיות הוא ציין. שטפו את האזור הפגוע עם הרבה מים וסבון.
- מגע ממושך העור מסיר את השומן הטבעי שלך, מפעילה דרמטיטיס.
- שאיפה יכולה לגרום למצב דמוי שפעת (אדים מתכתיים). המצב מאופיין חום גבוה, צמרמורות, יובש בפה יבש, כאבי שרירים וכאבי ראש.
- זה יכול לגרות את דרכי הנשימה ולהגדיל את השכיחות של זיהומים בדרכי הנשימה (דלקת ריאות). הרעלה על ידי ספיגה של מלחים מנגן אנאורגניים דרך הריאות היא לא סביר, אבל הרעלת כרונית יכולה להתרחש.
- חשיפה כרונית לאבק או לאדים של דו-תחמוצת המנגן לאורך זמן עלולה להשפיע על מערכת העצבים המרכזית ולהוביל להתפתחות מחלת פרקינסון, קשיי הליכה, התכווצויות שרירים ושינויים התנהגותיים.
- בליעה עלולה לגרום לכאבי בטן ובחילות.
- זה לא דליק, אבל זה עוזר להפיץ את האש בחומרים ליבון. אם מחומם לטמפרטורה מעל 535 ° C החומר מתפרק ל מנגן אוקסיד (III) Mn2הו3 ואת החמצן, שהוא דליק ומגביר את הסכנה של אש. במקרה זה יש לכבות את האש עם קצף או דו תחמוצת הפחמן.
- במקרה של שפיכה, אין לתפעל את המתחם ללא הגנה אישית נאותה.
- אחסן את המתחם במיכלים סגורים היטב, במקום קר ויבש, הרחק מחומרים שאינם תואמים כגון חומר אורגני וחומר דליק.
- מקום האחסון חייב להיות יבש ויש לו עמידות בפני קורוזיה חומצה עם ניקוז טוב..
- יש להשתמש בציוד מגן אישי, כגון כפפות, משקפי מגן, מסנני אנטי-אדים, אבק ועשן.
הפניות
- B, (2015), דו תחמוצת מנגן, החברה המלכותית לכימיה - עולם הכימיה, מתוך chemistryworld.com
- Karal, (2014), Mangneso Dioxide, גיליון נתוני בטיחות, משוחזר מ, karal.com.mx
- המורה הווירטואלי שלך (2015-02-25). תרכובות אנאורגניות של מנגן (מקרה מיוחד 1) - שיעור תיאורטי), נלקח מ- youtube.com
- Ecured, (s.f), דו תחמוצת מנגן, משוחזר מ ecured.cu
- אנגאריטה G, ג 'וני., (2017), דו תחמוצת מנגן: טכנולוגיה יוצאת דופן. הידרוטק, התאושש מ hydrotecocr.com
- פרננדז, ג ', (2015), MnO מנגן דו חמצני2/ אצטון, כימיה אורגנית, משוחזר מ quimicaorganica.net
- Tronox, (2011), דו תחמוצת מנגן, גיליון נתונים בטיחות, שחזר מ, tronox.com


