סידן אוקסיד (CaO) מבנה, נכסים ושימושים
ה תחמוצת סידן (CaO) הוא תרכובת אנאורגנית המכילה סידן וחמצן בצורות יוניים (לא להתבלבל עם סידן חמצן, CaO2). גלובלי זה נקרא סיד, מילה לכל תרכובת אורגנית המכילה קרבונטים, תחמוצות ו והידרוקסידים של סידן, ומתכות אחרות כגון סיליקון, אלומיניום וברזל.
זה תחמוצת (או סיד) הוא גם מכונה בדיבור כמו סיד או ליקח סיד, תלוי אם זה לא hydrated. סיד הוא תחמוצת סידן, בעוד סיד סיד הוא hydroxide שלה. בתורו, אבן גיר (אבן סיד או מוקשה סיד) הוא למעשה סלע משקע המורכב בעיקר של סידן פחמתי (CaCO3).

זהו אחד המקורות הטבעיים הגדולים של סידן ומהווה את חומר הגלם לייצור תחמוצת סידן. איך זה תחמוצת המיוצר? פחמנים הם רגישים פירוק תרמי; חימום סידן פחמתי בטמפרטורות מעל 825 מעלות צלזיוס, המוביל להיווצרות של סיד ופחמן דו חמצני.
את ההצהרה לעיל ניתן לתאר כדלקמן: CaCO3(ים) → CaO (ים) + CO2(ז) בגלל קרום כדור הארץ עשיר באבן גיר ו calcite, ועל האוקיינוסים והחופים הם שופע הים פגזים (חומרי גלם לייצור תחמוצת סידן), תחמוצת סידן מגיב זול יחסית.
אינדקס
- 1 נוסחה
- מבנה
- 3 מאפיינים
- 3.1 מסיסות
- 4 שימושים
- 4.1 כמכתש
- 4.2 בייצור משקפיים
- 4.3 בכרייה
- 4.4 כמסיר סיליקט
- 5 חלקיקים של תחמוצת סידן
- 6 הפניות
נוסחה
הנוסחה הכימית של תחמוצת סידן הוא CaO, שבו סידן הוא כמו יון חומצה (acceptor אלקטרונים) Ca2+, ואת החמצן כמו יון בסיסי (תורם אלקטרונים) או2--.
למה סידן יש תשלום 2? בגלל סידן שייכת לקבוצה 2 של הטבלה המחזורית (מר Becambara), ורק שתיים ערכי אלקטרונים זמינים עבור היווצרות קשר, אשר מניבה אטום החמצן.
מבנה
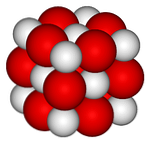
בתמונה העליונה, המבנה הגבישי (סוג פנינה מלח) עבור תחמוצת סידן מיוצג. הכדורים האדומים הרבים תואמים את היונים2+ ואת הספירות הלבנות אל היונים O2-.
זה סידור גביש מעוקב כל יון Ca2+ הוא מוקף שישה יונים O2-, חורים בחורים octahedral שהותיר יונים גדולים ביניהם.
מבנה זה מבטא את המקסימום את האופי היוני של תחמוצת זו, אם כי ההבדל המדהים של רדיוס (כדור אדום גדול יותר לבן אחד) מעניק אנרגטי הרשתית גבישית חלשה יותר בהשוואה MgO.
מאפיינים
פיזית, הוא גביש לבן מוצק, חסרות ריח חזק אינטראקציות אלקטרוסטטיות, אשר אחראים נקודות ההתכה הגבוהה שלהם (C ° 2572) ו הרתיחה (C ° 2850). בנוסף, בעל משקל מולקולרי של 55.958 g / mol ואת התכונה המעניינת של להיות thermoluminescent.
פירוש הדבר כי פיסת תחמוצת סידן שנחשפה להבה יכולה להאיר באור לבן עז, הידועה באנגלית עם השם אור הזרקורים, או בספרדית, אור של סידן. את יונים Ca2+, במגע עם האש, הם גורמים להבה אדמדמה, כפי שמוצג בתמונה הבאה.

מסיסות
CaO הוא תחמוצת בסיסית בעלת זיקה חזקה למים, במידה שהיא סופגת לחות (היא מוצקה היגרוסקופית), המגיבה מיד לייצור סיד או סידן הידרוקסיד:
קאו (ים) + H2O (l) => Ca (OH)2(ים)
תגובה זו היא אקסותרמית (משחררת חום) בשל היווצרות של מוצק עם אינטראקציות חזקות יותר סריג גביש יציב יותר. עם זאת, התגובה היא הפיך אם Ca (OH) מחומם2, מייבשת אותו ומדליקה את הסיד השרוע; אז, סיד "מחדש".
הפתרון שנוצר הוא בסיסי מאוד, ואם הוא רווי תחמוצת סידן הוא מגיע pH של 12.8.
כמו כן, הוא מסיס ב גליצרול ו חומצה סוכר פתרונות. כפי שהוא תחמוצת בסיסית, זה טבעי יש אינטראקציות אפקטיביות עם תחמוצות חומצה (SiO2, אל2הו3 ואת האמונה2הו3, למשל) להיות מסיסים בשלבים הנוזליים שלה. מצד שני, הוא מסיס באלכוהול וממיסים אורגניים.
שימושים
CAO יש מספר עצום של שימושים תעשייתיים, כמו גם סינתזה של אצטילן (CH≡CH), בהפקת פוספטים מן השפכים ובתגובה עם דו תחמוצת הגופרית מפסולת גזי..
שימושים אחרים של תחמוצת סידן מתוארים להלן:
כמרגמה
אם תחמוצת הסידן מעורבב בחול (SiO)2), מים, עוגות עם החול ומגיבה באיטיות עם המים ליצירת סיד מרופט. בתורו, המפקד2 של האוויר מתמוסס במים ומגיב עם המלח כדי ליצור סידן פחמתי:
Ca (OH)2(ים) + CO2(g) => CaCO3(ים) + H2O (l)
הקאקו3 קשוחה ונוקשה הוא מאשר תרכובת קאו, גורמת מרגמה (את התערובת מעל) להקשיח ולתקן את לבנים, בלוקים קרמיים או בין אלה או על פני השטח הרצוי.
בייצור משקפיים
חומר הגלם חיוני לייצור משקפיים הם תחמוצות סיליקון, אשר מעורבים עם סיד, פחמתי נתרן (Na2CO3) ותוספים אחרים, ולאחר מכן להיות נתון חימום, וכתוצאה מכך מוצק זכוכית. זה מוצק הוא מחומם לאחר מכן פוצצו בכל הדמויות.
בכרייה
סיד ליקח תופסת נפח גדול יותר מאשר quicklime עקב מליטה מימן (O-H-O) אינטראקציות. מאפיין זה משמש לשבור את הסלעים מבפנים.
זו מושגת על ידי מילוי אותם עם תערובת קומפקטית של סיד ומים, אשר אטום כדי למקד את החום ואת הכוח המרחבי בסלע.
כמסיר סיליקט
CaO הוא התמזגו עם silicates כדי ליצור נוזל coalscent, אשר מופק מכן מחומר גלם של מוצר מסוים.
לדוגמה, עפרות ברזל הם חומר גלם לייצור ברזל ופלדה מתכתי. מינרלים אלה מכילים silicates, אשר זיהומים לא רצויים עבור תהליך והם בוטלו על ידי השיטה רק תיאר.
חלקיקים של תחמוצת סידן
תחמוצת סידן יכול להיות מסונתז כמו חלקיקים, שינוי הריכוזים של סידן חנקה (Ca (NO3)2) ו hydroxide נתרן (NaOH) בפתרון.
חלקיקים אלה הם כדוריים, בסיסיים (כמו גם מאקרו בקנה מידה מוצק) ויש להם הרבה שטח הפנים. כתוצאה מכך, תכונות אלה לטובת תהליכי קטליטי. אשר החקירות עונות כעת על שאלה זו.
חלקיקים אלה שימשו לסינתזה של תרכובות אורגניות תחליף - הנובעות מפירדינים - בניסוח של תרופות חדשות לביצוע שינויים כימיים כגון פוטוסינתזה מלאכותית, לטיהור מים ממתכות כבדות ורעילות, וכן סוכני פוטוקטליטיים.
חלקיקים יכול להיות מסונתז על תמיכה ביולוגית, כגון עלים של פפאיה ותה ירוק, לשמש כסוכן אנטיבקטריאלי.
הפניות
- scifun.org (2018). סיד: תחמוצת סידן. אחזור ב -30 במרץ 2018, מתוך: scifun.org.
- ויקיפדיה. (2018). תחמוצת סידן. אחזור ב -30 במרץ 2018, מ: en.wikipedia.org
- Ashwini Anantharaman et al. (2016). סינתזה ירוקה של סידן אוקסיד חלקיקים ויישומיה. Int. Journal of הנדסה מחקר ויישום. ISSN: 2248-9622, Vol. 6, Issue 10, (Part -1), pp.27-31.
- ג'יי Safaei-גהומי ואח. (2013). חלקיקי תחמוצת סידן מזורזת pyridines סינתזה של multicomponent צעד אחד הוחלף התקשורת מימית מאוד אתנול Scientia Iranica, עסקאות C: כימיה הנדסה כימית 20 549-554.
- PubChem. (2018). תחמוצת סידן. ב -30 במרץ 2018, מתוך: pubchem.ncbi.nlm.nih.gov
- צמרמורת & אטקינס. (2008). כימיה אנאורגנית ב אלמנטים של קבוצה 2. (מהדורה רביעית, עמ '280). מק גרב היל.


