מלחים אורגניים תכונות פיסיקליות וכימיות, שימושים ודוגמאות
ה מלחנים אורגניים הם מספר צפוף של תרכובות יוניות עם מאפיינים אין ספור. הם נובעים קודם לכן מתחם אורגני, שעבר טרנספורמציה המאפשרת לו להיות נושא של מטען, וכי גם הזהות הכימית שלו תלויה ביון המשויך.
בתמונה להלן שתי נוסחאות כימיות כלליות מאוד עבור מלחי אורגני מוצגים. הראשון, R-AX, מתפרש כתרכובת שבה מבנה הפחמן אטום, או קבוצה A, נושא חיוב חיובי + או שלילי (-).
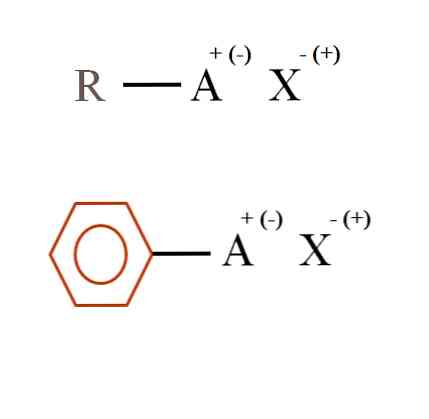
כפי שניתן לראות, קיים קשר קוולנטי בין R ו- A, R-A, אבל בתורו, א 'הוא מטען פורמלי שמושך (או דוחה) את X. יון הסימן של המטען תלוי באופיו של A ו- הסביבה הכימית.
אם A היו חיוביות, כמה X יכול לתקשר עם זה? עם רק אחד, בהתחשב בעקרון electroneutrality (+ 1-1 = 0). עם זאת, מהי הזהות של X? אניון X יכול להיות CO32-, המחייבת שתי קטיונים+; הלוגניד: F-, Cl-, בר-, וכו '; או אפילו, תרכובת RA נוספת-. האפשרויות הן בלתי ניתנות לחישוב.
כמו כן, מלח אורגני יכול להיות בעל אופי ארומטי, מאויר בטבעת בנזין חום. מלח בנזואט נחושת (II), (C6ח5COO)2Cu, למשל, מורכב משני טבעות ארומטיות עם קבוצות carboxyl טעונים שלילית, אשר אינטראקציה עם Cu קטיון.2+.
אינדקס
- תכונות פיסיקליות וכימיות
- 1.1 מסה מולקולארית גבוהה
- 1.2 Amphiphiles ו פעילי שטח
- 1.3 נקודות רתיחה גבוהות או היתוך
- 1.4 חומציות וסיסיים
- 2 שימושים
- 3 דוגמאות למלחים אורגניים
- 3.1 קרבוקסילטים
- 3.2 ליתיום diacryluprates
- 3.3 מלחים של סולפוניום
- 3.4 מלחים של אוקסיום
- 3.5 מלחי אמין
- 3.6 מלח דיזוניום
- 4 הפניות
תכונות פיסיקליות וכימיות
תמונה ניתן לומר כי המלחים האורגניים מורכבים משלושה מרכיבים: האורגני, R או אר (טבעת ארומטית), נושאת אטומה או יון גובי קבוצה, וכן counterion X.
בדיוק כמו זהות כימית ומבנה מוגדרים על ידי רכיבים כאלה, ולכן המאפיינים שלהם תלויים בהם.
מתוך עובדה זו ניתן לסכם תכונות כלליות מסוימות העונות על הרוב המכריע של אלה מלחים.
המוני מולקולרי גבוה
בהנחה של monon או polyvalent X אניונים anorganic, מלחי אורגני בדרך כלל יש הרבה יותר המונית מולקולרית מאשר מלחים אנאורגניים. זה בעיקר בשל שלד פחמן, אשר פשוט C-C האג"ח, ואת אטומי מימן שלהם, לתרום המון המוני למתחם.
לכן, הם R או Ar אחראי משקולות מולקולריות גבוהות שלהם.
אמפיפיל ועמילנים
מלחי אורגני הם תרכובות amphiphilic, כלומר, המבנים שלהם יש הן hydrophilic ו הידרופובי.
מה הם קיצוניים כאלה? R או Ar מייצגים את קצה הידרופובי, כי אטומים C ו- H שלהם אין זיקה רבה עבור מולקולות מים.
א+(-), אטום או קבוצה נושאת את המטען, הוא סוף hydrophilic, שכן הוא תורם רגע dipolar ו אינטראקציה עם מים להרכיב dipoles (RA+ הו2).
כאשר אזורים הידרופילי והידרופובי מקוטבים, מלח amphiphilic הופך פעילי שטח, חומר בשימוש נרחב לייצור דטרגנטים ו דולסיפיר.
גבוה רותחים או נקודות ההיתוך
כמו מלחים אנאורגניים, מלחי אורגני גם יש התכה גבוהה נקודות רתיחה, בשל כוחות אלקטרוסטטיים השולטים בשלב נוזלי או מוצק.
עם זאת, בעל R מרכיב אורגני או אר, מעורבים סוגים אחרים של קשרי ואן דר ואלס (כוחות בלונדון, דיפול דיפול, קשרי מימן) כי להתחרות בצורה מסוימת עם אלקטרוסטטית.
מסיבה זו, מבנים מוצקים או נוזליים של מלחי אורגני הם, במקרה הראשון, מורכב יותר ומגוון. כמה מהם יכולים אפילו להתנהג כמו גבישים נוזליים.
חומציות בסיסיות
מלחי אורגני הם בדרך כלל חומצות חזקות יותר או בסיסים מאשר מלחים אנאורגניים. הסיבה לכך היא A, למשל של מלחי אמין, יש חיוב חיובי בשל הקשר שלה עם מימן נוסף: א+-H. לאחר מכן, במגע עם בסיס, לתרום את הפרוטון לחזור להיות מתחם ניטרלי:
RA+H + B => RA + HB
ה- H שייך ל- A, אך הוא כתוב כפי שהוא מתערב בתגובת הניטרול.
מצד שני, RA+ זה יכול להיות מולקולה גדולה, מסוגל ליצור מוצקים עם רשת גבישית יציבה מספיק עם הידרוקסיל אניון או הידרוקסיל OH-.
כאשר זה המקרה, מלח RA+הו- זה מתנהג כמו בסיס חזק; אפילו בסיסי כמו NaOH או KOH:
RA+הו- + HCl => RACl + H2הו
שימו לב במשוואה הכימית כי אניון Cl- זה מחליף את OH-, ויצרו מלח מלח+Cl-.
שימושים
השימוש במלחי אורגני ישתנה בהתאם לזהותם של R, Ar, A ו- X. יתר על כן, היישום אליו הם מיועדים גם תלוי בסוג מוצק או נוזל שהם יוצרים. כמה הכללים בהקשר זה הם:
-הם משמשים ריאגנטים לסינתזה של תרכובות אורגניות אחרות. RAX יכול לשמש "התורם" של שרשרת R כדי להוסיף למתחם אחר להחליף קבוצה יוצאת טובה.
-הם פעילי שטח, ולכן הם יכולים לשמש גם חומרי סיכה. מלחי מתכת של carboxylates משמשים למטרה זו.
-הם מאפשרים לסנתז מגוון רחב של צבעים.
דוגמאות למלחים אורגניים
Carboxylates
חומצות carboxylic להגיב עם hydroxide בתגובת נייטרלי, המביא את מלחים של carboxylates: RCOO- M+; שבו M+ זה יכול להיות כל קטיון מתכת (Na+, Pb2+, K+, וכו ') או קטיון אמוניום NH4+.
חומצות שומן הן שרשרת ארוכה של חומצות קרבוקסיליות אליפטיות, הן יכולות להיות רוויות ולא רוויות. חומצה Palmitic (CH) הוא בין רווי3(CH2)14COOH). זה מקורו מלח palmitate, בעוד חומצה סטארית (CH3(CH2)16COOH יוצר את מלח stearate. הסבונים מורכבים מלחים אלה.
במקרה של חומצה בנזואית, C6ח5COOH (כאשר C6ח5- זה טבעת בנזן), כאשר הוא מגיב עם בסיס טפסים מלחי בנזואט. בכל carboxylates, קבוצת COO- מייצג A (RAX).
ליתיום diacupuprates
ליתיום diacuprate שימושי סינתזה אורגנית. הנוסחה שלה היא [R-Cu-R]-לי+, שבו אטום הנחושת נושא מטען שלילי. הנה, נחושת מייצג את האטום A של התמונה.
מלחי סולפוניום
הם נוצרים מתגובה של גופרית אורגנית עם הליק אלקיל:
R2S + R'X => R2R+X
עבור מלחים אלה, אטום גופרית נושאת מטען חיובי חיובי (S+) בעל שלוש קוולנטים.
מלחי אוקסוניום
כמו כן, אתים (האנלוגים מחומצן של סולפידים) להגיב עם hydrocides כדי ליצור את מלחי אוקסוניום:
ROR '+ HBr <=> RO+HR + + Br-
חומצה פרוטון של HBr קשורה קוולנטית לאטום החמצן של האתר (R2הו+-H), טוען אותו באופן חיובי.
מלחי אמין
האמינים יכולים להיות ראשוניים, משניים, שלישוני או רביעוני, כמו גם מלחים שלהם. כולן מאופיינות באטום H הקשור לאטום החנקן.
אז, RNH3+X- הוא מלח אמין העיקרי; R2NH2+X-, של אמין משני; R3NH+X-, של אמין שלישוני; ו- R4N+X-, של quaternary אמין (מלח רביעוני אמוניום).
מלחי דיאזוניום
לבסוף, מלחי דיאזוניום (RN2+X-) או arildiazonium (Arn)2+X-), מייצגים את נקודת המוצא עבור תרכובות אורגניות רבות, במיוחד צבעי azo.
הפניות
- פרנסיס א. כימיה אורגנית (מהדורה שישית, עמ '604-605, 697-698, 924). מק גרב היל.
- גרהם סולומונס ט. וו. קרייג ב. פרייהל. כימיה אורגנית. Amines (מהדורה 10). ויילי פלוס.
- ויקיפדיה. (2018). מלח (כימיה). מתוך: en.wikipedia.org
- סטיבן א. הרדינגר. (2017). מילון מונחים של כימיה אורגנית: מלחים. מקור: chem.ucla.edu
- שברון אורוניט. (2011). Carboxylates. [PDF] מקור: oronite.com


