חוק של בויל- Mariotte ההיסטוריה, ביטוי מתמטי, דוגמאות
חוק בויל-מריוט היא זו המבטאת את היחס בין הלחץ המופעל על ידי הגז ובין על כמותו; שמירה קבועה על טמפרטורת הגז, כמו גם כמות (מספר שומות).
חוק זה, יחד עם זה של צ'רלס, גיי-לוסאק, צ'רלס ואבוגדרו, מתאר את התנהגותו של גז אידיאלי; במיוחד, במיכל סגור נתון לשינויים בנפח המופעל על ידי כוח מכני.
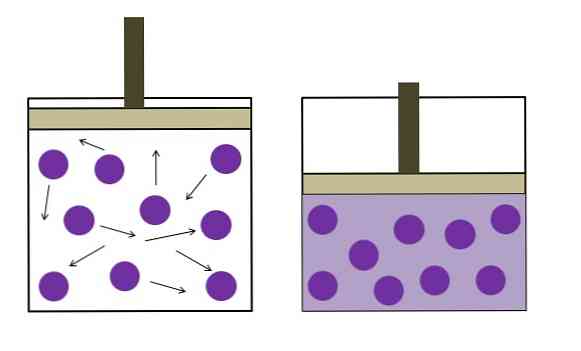
התמונה לעיל מסכם בקצרה את חוק בויל-מריוט.
הנקודות הסגולות מייצגות מולקולות או אטומי גז, אשר מתנגשות עם הקירות הפנימיים של המכולה (משמאל). על ידי הקטנת שטח או נפח זמין של המיכל שנכבשו על ידי גז זה, התנגשויות להגדיל, אשר מתרגמת לעלייה בלחץ (מימין).
זה מראה כי הלחץ P ונפח V של הגז הם ביחס הפוך אם מיכל אטום הרמטית; אחרת, לחץ גבוה יותר יהיה שווה להרחבה גדולה יותר של המכולה.
אם בוצעה העלילה V נגד P, עם נתוני V ו- P על ציר Y ו- X, בהתאמה, עקומת אסימפטוטית תיראה. ככל ש - V קטן יותר, כך גדל ה - P; כלומר, העקומה תרחיב לערכים גבוהים של P על ציר ה- X.
כמובן, הטמפרטורה נשארת קבועה; אבל, אם אותו ניסוי בוצע בטמפרטורות שונות, את המיקום היחסי של עקומות אלה V לעומת P ישתנה ציר קרטזית. השינוי יהיה בולט עוד יותר אם יוכנס על ציר תלת מימדי, עם ציר קבוע על ציר ה- Z.
אינדקס
- 1 היסטוריה של חוק בויל
- 1.1 רקע
- 1.2 ניסוי כספית
- 1.3 אדמה מריוט
- 1.4 חיזוק החוק
- 2 מה זה החוק מורכב??
- 3 ביטוי מתמטי
- 4 מה זה? אילו בעיות פותח חוק בויל??
- 4.1 מכונות קיטור
- 4.2 לגם משקאות
- 4.3 מערכת הנשימה
- 5 דוגמאות (ניסויים)
- 5.1 ניסוי 1
- 5.2 ניסוי 2
- 6 הפניות
היסטוריה של חוק בויל
רקע
מאז המדען גלילאו גליליי הביע את אמונתו בקיומה של ריקנות (1638), מדענים החלו ללמוד את המאפיינים של האוויר והחללים החלקיים.
הרוקח האנגלו-אירי, רוברט בויל, החל את מחקרו על נכסי האוויר ב -1638 כשנודע לו שאוטו פון גריקה, מהנדס ופיסיקאי גרמני, בנה משאבת אוויר.
ניסוי עם כספית
כדי לבצע את מחקריו על לחץ האוויר, השתמש בויל בצינור זכוכית בצורת "J", שבנייתו יוחסה לרוברט הוק, עוזרו של בויל. קצה הזרוע הקצרה היה אטום, ואילו קצה הזרוע הארוכה של הצינור היה פתוח למקם את הכספית.
מלכתחילה רצה בויל לחקור את גמישות האוויר, איכותית וכמותית. על ידי שפכו כספית דרך הקצה הפתוח של צינור "J" בצורת, מסיק בויל כי האוויר בזרוע הקצר של הצינור התכווץ תחת לחץ כספית.
תוצאות
ככל שכספית הכספית מתווספת לצינור, כך גדל הלחץ המופעל על האוויר והנפח נמוך יותר. בויל השיג גרף סוג אקספוננציאלי של נפח האוויר כפונקציה של לחץ.
אמנם, אם אתה מגרש את נפח האוויר כנגד ההופכי של הלחץ, יש לך קו ישר של שיפוע חיובי.
בשנת 1662 פרסם בויל את החוק הפיזי הראשון שניתן במשוואה, אשר הצביע על התלות הפונקציונלית של שני משתנים. במקרה זה, הלחץ והנפח.
בויל הצביע על כך שיש קשר הפוך בין הלחץ המופעל על הגז לבין הנפח הכבוש בגז זה, יחס זה נכון יחסית לגזים אמיתיים. רוב הגזים מתנהגים כמו גזים אידיאליים בלחצים מתונים וטמפרטורות.
עם לחצים גבוהים יותר וטמפרטורות נמוכות יותר, חריגות מהתנהגות הגזים האמיתיים של האידיאלים נעשו בולטים יותר.
אדמה מריוט
הפיזיקאי הצרפתי אדמה מריוט (1620-1684) גילה באופן עצמאי את אותו חוק בשנת 1679. אבל היה לו את הכשרון להראות כי נפח משתנה עם הטמפרטורה. לכן זה נקרא החוק של מריוט או של בויל ושל חוק מריוט.
חיזוק החוק
דניאל ברנולי (1737) חיזק את חוק בויל בהצביע על כך שהלחץ של גז מופק על ידי השפעות של חלקיקי גז על קירות המיכל המכיל אותו..
בשנת 1845 פרסם ג'ון ווטרסטון מאמר מדעי, שבו הוא מתמקד בעקרונות המרכזיים של התיאוריה הקינטית של גזים.
מאוחר יותר, רודולף קלאוזיוס, ג'יימס מקסוול ולודקוויג בולצמן איחדו את התיאוריה הקינטית של גזים, אשר מייחסת את הלחץ המופעל על ידי גז, עם מהירות של חלקיקי הגז בתנועה.
ככל שכמות המיכל המכילה גז קטנה יותר, כך גדל תדירות השפעתם של החלקיקים המרכיבים אותו על קירות המכולה; ולכן, כך גדל הלחץ המופעל על ידי הגז.
מה החוק הזה מורכב??
הניסויים שבוצעו על ידי בויל מציינים כי קיים קשר הפוך בין נפח הכבושה על ידי גז לבין הלחץ המופעל על זה. עם זאת, היחסים הנ"ל הוא לא ליניארי לחלוטין, כפי שניתן לראות על ידי גרף של וריאציה נפח לפי הלחץ המיוחס בויל.
בחוק בויל צוין כי נפח הכבוש על ידי גז הוא ביחס הפוך ללחץ. כמו כן צוין כי תוצר הלחץ של גז בכמותו קבוע.
ביטוי מתמטי
כדי להגיע לביטוי המתמטי של חוק בויל-מריוט, אנו מתחילים מתוך:
V α 1 / P
כאשר הוא מציין כי נפח הכבוש על ידי גז הוא ביחס הפוך ללחץ שלה. עם זאת, יש קבוע המכתיב כמה יחסי הפוך זה היחסים.
V = k / P
כאשר k הוא קבוע המידתיות. ניקוי k יש לך:
סגן נשיא = k
תוצר הלחץ של גז בכמותו קבוע. ואז:
אשר1עמ '1 k ו- V2עמ '2 = k
ומכאן ניתן להסיק כי:
אשר1עמ '1 49 אשר2עמ '2
האחרון הוא הביטוי הסופי או משוואה לחוק בויל.
בשביל מה? אילו בעיות פותח חוק בויל??
מכונות קיטור

חוק בויל-מריוט חל על הפעלתם של מנועי קיטור. זהו מנוע בעירה חיצוני המשתמש בהפיכת אנרגיה תרמית מכמות מים לאנרגיה מכנית.
המים מחוממים בדוד אטום הרמטית, והאדים המופקים מפעילים לחץ על פי חוק בויל-מריוט שמייצר הרחבה של גליל על ידי דחיפת בוכנה.
התנועה הליניארית של הבוכנה הופכת לתנועה סיבובית, באמצעות שימוש במערכת של cranks ו cranks, אשר יכול לנהוג את הגלגלים של קטר או את הרוטור של גנרטור חשמלי.
כיום, מנוע הקיטור האלטרנטיבי הוא מנוע קטן המשמש, שכן הוא נעקר על ידי המנוע החשמלי ואת מנוע הבעירה הפנימית בכלי תחבורה.
לוגמים משקאות
הפעולה של מציצה של משקה קל או מיץ מבקבוק דרך צינור פלסטיק קשורה לחוק בויל-מריוט. כאשר האוויר נשאב מן הצינור באמצעות הפה, יש ירידה בלחץ בתוך הצינור.
זו ירידה בלחץ מקל על התנועה כלפי מעלה של הנוזל בצינור, המאפשר את הבליעה שלה. זה אותו עיקרון עובד בהפקת הדם באמצעות מזרק.
מערכת הנשימה
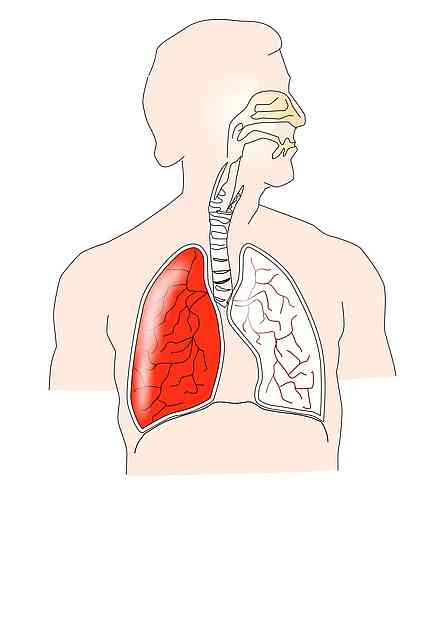
חוק בויל-מריוט קשור באופן הדוק לתפקוד מערכת הנשימה. בשלב ההשראה מתרחש התכווצות של הסרעפת ושרירים אחרים; למשל, intercostals חיצוני המייצרים הרחבה של כלוב הצלעות.
זה גורם לירידה בלחץ intrapleural, אשר גורם להרחבת הריאות המייצרת גידול בנפח הריאות. לכן, הלחץ intrapulmonary פוחת בהתאם לאמור בחוק בויל-מריוט.
כאשר הלחץ intrapulmonary הוא subatmospheric, אוויר אטמוספרי זורם לתוך הריאות, וכתוצאה מכך לחץ מוגבר הריאות; השווה, הלחץ שלה ללחץ אטמוספרי, וסיום שלב ההשראה.
לאחר מכן, השרירים השראה להירגע השרירים expiratory החוזה. בנוסף, מתרחשת נסיגה אלסטית ריאתי, תופעה שמייצרת ירידה בנפח הריאות, עם עלייה עקבית בלחץ תוך-גולגולתי, אשר ניתן להסביר על ידי חוק בויל-מריוט..
על ידי הגדלת הלחץ intrapulmonary, ולהיות גדול יותר מאשר לחץ אטמוספרי, האוויר זורם מתוך הריאות לתוך האווירה. זה קורה עד הלחצים הם השווה, אשר מסכם את שלב התפוגה.
דוגמאות (ניסויים)
ניסוי 1
בלון קטן ממוקם בחוזקה סגור, מה שהופך קשר בפה, בתוך מזרק, אשר הבוכנה הוסרה, של כ 20 מ"ל. הבוכנה של המזרק ממוקמת לכיוון החלק המרכזי של המזרק, המחט מוסרת ואת כניסת האוויר נחסמה.
תצפית
לאט לאט משיכת הבוכנה של המזרק, הוא ציין כי הבלון מנופח.
הסבר
שני לחצים מופעלים על קיר הבלון: לחץ על פניו הפנימיות, תוצר האוויר הכלול בתוך הבלון, ולחץ נוסף על פני הבלון החיצוניים, המופעל על ידי האוויר הכלול במזרק.
כאשר מושך את הבוכנה של המזרן, נוצר חצי ואקום בתוכו. לכן, לחץ האוויר על הפנים החיצוניים של קיר המשאבה פוחתת, מה שהופך את הלחץ המופעל בתוך המשאבה גדול יחסית..
לחץ זה, על פי חוק בויל-מריוט, יפיק התמתנות של קיר הבלון וגידול בנפח הבלון.
ניסוי 2
חותכים בקבוק פלסטיק, בערך במחצית, ולוודא כי לחתוך הוא אופקי ככל האפשר. בפה של הבקבוק ממוקם בלון מותאם היטב, באותו זמן כמות מסוימת של מים מונח בצלחת עמוקה.
תצפית
על ידי הנחת תחתית הבקבוק עם הבלון על המים של המנה, הבלון מנופח למדי.
הסבר
המים מחליפים כמות מסוימת של אוויר, מגדילים את לחץ האוויר על קיר הבקבוק ועל פנים הבלון. זה גורם, על פי החוק של בויל- Mariotte, עלייה בנפח של העולם, אשר דמיינו האינפלציה של כדור הארץ.
הפניות
- ויקיפדיה. (2019). חוק בויל. מקור: en.wikipedia.org
- עורכי האנציקלופדיה בריטניקה. (27 ביולי 2018). חוק בויל. אנציקלופדיה בריטניקה. מקור: britannica.com
- הלמנסטיין, טוד. (5 בדצמבר 2018). נוסחאות חוק בויל. מקור: Thinkco.com
- סרטים הודיים צעירים. (15 במאי 2018). חוק בויל: ניסוי מדע לילדים. מקור: yifindia.com
- ססיליה במביבר (22 במאי 2011). כדור פורח הגדרה ABC. מקור:
- Ganong, W, F. (2003). פיזיולוגיה רפואית (מהדורה 19). העריכה של המדריך המודרני.


