סודיום הידריד (NaH) מאפיינים, תגובתיות, סיכונים ושימושים
ה סודיום הידריד הוא תרכובת אנאורגנית של נוסחת NaH. יש לה קשר יוני בין נתרן להידריד. המבנה שלה מתואר באיור 1. הוא מייצג הידרידים מלוחים, כלומר, הידריד דומה למלח, המורכב מנא + ו-יונים, בניגוד הידרידס המולקולריים יותר כגון בוראן, מתאן, אמוניה ומים.
במבנה הגבישים יש מספר תיאום 6, שבו כל מולקולת נתרן מוקפת ב -8 יונים הידרידיים בעלי צורה אוקטדרלית ומודגם באיור 2 (מארק ווינטר [אוניברסיטת שפילד ו- WebElements Ltd, 1993-2016].
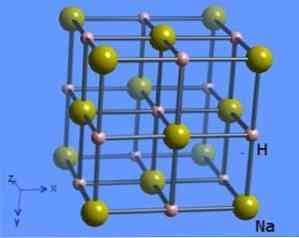
המתקן מוכן על ידי התגובה הישירה בין נתרן ומימן גז (סודיום הידריד פורמולה - סודיום הידריד שימושים, נכסים, מבנה ופורמולה, 2005-2017) כדלקמן:
H2 + 2Na → 2NaH
נתרן הידריד נמכר באופן מסחרי כמו 60% w / w פיזור צורה (משקל עבור משקל אחוז) בשמן מינרלי לטיפול בטוח (SODIUM HYDRIDE, s.f).
אינדקס
- 1 תכונות פיסיקליות וכימיות של הידריד נתרן
- 2 תגובה וסיכונים
- 3 שימושים
- 4 הפניות
תכונות פיסיקליות וכימיות של נתרן הידריד
הידריד הנתרן הוא מוצק לבן כאשר הוא טהור למרות שהוא מתקבל בדרך כלל אפור או כסף. הופעתו מופיעה בתרשים 3.

NaH יש משקל מולקולרי של 23.99771 גרם / מול, צפיפות של 1.396 גרם / מ"ל נקודת התכה של 800 מעלות צלזיוס (החברה המלכותית לכימיה, 2015). זה לא מסיס אמוניה, בנזן, פחמן tetrachloride ו פחמן דיסולפיד (המרכז הלאומי למידע ביוטכנולוגיה, s.f.).
המתחם הוא מאוד לא יציב. Pure NaH יכול בקלות להצית באוויר. כאשר זה בא במגע עם המים נוכח באוויר, הוא משחרר מימן דליק מאוד.
כאשר פתוח לאוויר ולחות, NaH הוא גם hydrolyzed בקלות לתוך בסיס קורוזיבי חזק של נתרן hydroxide (NaOH) על פי התגובה:
NaH + H2O → NaOH + H2
בתגובה זו ניתן לראות כי hydride נתרן מתנהג כמו בסיס. זאת בשל electronegativity.
נתרן יש electronegativity נמוך משמעותית (≈1.0) מאשר מימן (≈ 2.1), כלומר מימן תמציות צפיפות האלקטרונים כלפי עצמו, מתרחק נתרן ליצור קטיון נתרן ו אניון של הידריד.
עבור תרכובת להיות חומצה Brønsted, זה צריך להפריד את צפיפות האלקטרונים מן המימן, כלומר, לחבר אותו אטום electronegative כגון חמצן, פלואור, חנקן, וכו ' רק אז, ניתן לתאר את זה באופן רשמי כ- H +, וניתן לנתק אותו ככזה.
הידריד הוא הרבה יותר טוב כפי שתואר H - ויש לו זוג אלקטרונים חינם. ככזה, זה בסיס Brønsted, לא חומצה. למעשה, אם אתה מרחיב את החומצה Brunnsted / הגדרה בסיס בדרך לואיס עשה, תגיע למסקנה כי נתרן (Na +) הוא מינים חומצה כאן.
החומצה Brunnsted / בסיס התגובה המוצר של H- בסיס וחומצה H + הופך H2. בגלל מימן חומצה מופק ישירות מן המים, גז המימן יכול הבועה, העקירה את שיווי המשקל גם אם התגובה לא מעדיף תרמודינמית.
OH- יונים ניתן להשאיר כי ניתן לכתוב עם שאר קטיון Na לתת נתרן hydroxide (למה הוא מוצק נתרן הידריד מבוסס ולא חומצה כאשר הגיב עם מים ?, 2016).
תגובה וסיכונים
המתחם הוא סוכן הפחתת עוצמה. התקפות SiO2 בזכוכית. זה מתלקח על מגע עם F2 גז, Cl2, Br2 ו I2 (האחרון בטמפרטורות מעל 100 מעלות צלזיוס), במיוחד בנוכחות של לחות, כדי ליצור HF, HCl, HBR ו- HI.
מגיב עם גופרית לתת Na2S ו H2S. זה יכול להגיב בצורה נפוצה עם דימתיל sulfoxide. מגיב במרץ עם אצטילן, אפילו ב -60 ° C. זה דליק באופן ספונטני פלואור.
הוא יוזם תגובה פילמור ב ethyl-2,2,3-trifluoropropionate, כך האסטר מתפרק באלימות. נוכחות התגובה של diethyl succinate ו ethf trifluoroacetate, גרמה פיצוצים (SODIUM HYDRIDE, 2016).
הידריד נתרן נחשב קורוזיבי לעור או לעיניים, בשל הפוטנציאל של תוצרי לוואי של תגובות של מים עם מים.
במקרה של מגע עם העיניים, יש לשטוף אותם בכמויות גדולות של מים מתחת לעפעפיים לפחות 15 דקות ולבקש טיפול רפואי מיידי..
במקרה של מגע עם העור, צחצוח מידית ושטוף את האזור הפגוע במים. חפשו טיפול רפואי אם הגירוי נמשך.
זה מזיק על ידי בליעה עקב התגובה למים. אין לגרום להקאה. עליך לפנות מיד לטיפול רפואי ולהעביר את הקורבן למרכז רפואי.
הפיזור של נתרן הידריד בשמן הוא לא אבק. עם זאת, החומר המגיב יכול לפלוט ערפל מאכל בסדר. במקרה של שאיפה, לשטוף את הפה עם מים ולהעביר את הקורבן למקום עם אוויר צח. יש לחפש טיפול רפואי (Rhom and Hass Inc, 2007).
שימושים
השימוש העיקרי של hydride נתרן הוא לבצע עיבוי התגובות אלקילציה המתפתחים באמצעות היווצרות של קרבון (מזרז על ידי הבסיס).
סודיום הידריד בשמן דומה סודיום ונתרן מתכת alcoholates, ביכולתה לתפקד כסוכן deprotonating ב אסתר acetoacetic, Claisen, Stobbe, Dieckmann ותגובות אחרות הקשורות. יש לה יתרונות על פני סוכני עיבוי אחרים בכך:
- זהו בסיס חזק יותר, וכתוצאה מכך יותר deprotonation ישיר.
- לא נדרשת עודף.
- H2 מיוצר נותן מידה של מידת התגובה.
- תגובות משניות כגון הפחתות מסולקות.
Alkylations של amines ארומתית ו heterocyclic כגון 2-aminopyridine ו phenothiazine מושגות בקלות תשואה גבוהה באמצעות תערובות של toluene-methylformamide. ריכוז dimethylformamide הוא משתנה המשמש לשליטה על קצב התגובה (HINCKLEY, 1957).
השימוש hydride נתרן לאחסון של מימן לשימוש בתאי דלק דלק הוצע, hydride להיות מוקף גרגרי פלסטיק כי הם כתוש בנוכחות מים כדי לשחרר את המימן.
הפניות
- HINCKLEY, M. (1957). ייצור, טיפול, ושימושים של הידרידי הנתרן. הקדמה בכימיה, כרך י, 106-117.
- מארק וינטר [אוניברסיטת שפילד ו WebElements בע"מ, U. (1993-2016). נתרן: נתרן הידריד. מאוחזר WebElements: webelements.com.
- המרכז הלאומי למידע ביוטכנולוגי. (s.f.). מסד הנתונים PubChem Compound; CID = 24758. מקור: Pubchem: pubchem.ncbi.nlm.nih.gov.
- רום והוס inc. (2007, דצמבר). נתרן הידריד 60% פיזור בשמן. מאוחזר מ- dow.com.
- החברה המלכותית לכימיה. (2015). סודיום הידריד. מתוך ChemSpider: chemspider.com.
- סודיום היידריד. (2016). מקורו בקמיוכימיקלים:.
- סודיום הידריד פורמולה - הידריד נתרן שימושים, מאפיינים, מבנה ופורמולה. (2005-2017). מתוך Softschools.com: softschools.com.
- סודיום היידריד. (s.f.). מתוך Chemicalland21: chemicalland21.com.
- למה הוא מוצק נתרן hydride מבוסס ולא חומצה כאשר הגיב עם מים? (2016, 20 באפריל). מאוחזר מ stackexchange: chemistry.stackexchange.com.


