אלומיניום כלוריד (AlCl3) מבנה כימי, תכונות, משתמש
ה אלומיניום כלורי או אלומיניום trichloride (AlCl3) הוא מלח בינארי שנוצר על ידי אלומיניום וכלור. לפעמים זה נראה כמו אבקה צהובה כי זה מציג זיהומים בשל נוכחותו של ברזל (III) כלוריד.
הוא מתקבל על ידי שילוב האלמנטים שלו. אלומיניום, אשר יש שלושה אלקטרונים ברמת האנרגיה האחרונה שלה (משפחה IIIA), נוטה להניב אותם בשל אופי מתכתי שלה. כלור עם שבעה אלקטרונים ברמת האנרגיה האחרונה שלו (משפחה VIIA) נוטה לקבל אותם כדי להשלים octet שלה.
זה נחשב כי הקשר שנוצר בין אלומיניום כלור אלומיניום trichloride הוא קוולנטי, למרות שזה האיגוד בין מתכת שאינם מתכת.
ישנם שני סוגים של כלוריד אלומיניום:
- אלומיניום כלוריד נטול מים. AlCl3.
- אלומיניום כלוריד הקסאהידראט. AlCl3. 6H2O. המתחם הזה ניתן למצוא בצורת מוצק או פתרון.
אינדקס
- מבנה כימי
- 2 מאפיינים
- 2.1 פיזית
- 2.2 כימיקלים
- 3 שימושים
- 4 סיכונים: השפעות אפשריות
- 5 המלצות
- 6 הפניות
מבנה כימי
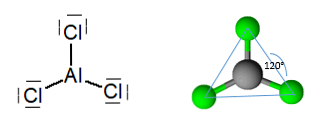
אלומיניום טריכלוריד נטול מים, הוא מולקולה עם גיאומטריה מישורית מישורית, עם זווית של 120 ° המקביל הכלאה האטומית sp2.
עם זאת, המולקולה מאורגנת בצורה של דימרס, שבו אטום כלור תורם זוג אלקטרונים כדי ליצור קשרים. אלה ידועים כאג"ח קוולנטיים מתואמים.
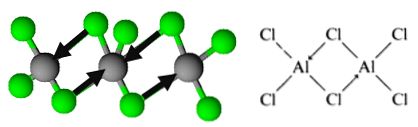
כך הארגון של dimers trichloride אלומיניום הוא deduced.
ארגון זה מאפשר למתחם ליצור רשתות של שכבות dimeric. כאשר המים נשפך על trichloride אלומיניום מוצק הם לא לנתק כצפוי מן המרכיבים היוניים, אבל עובר הידרוליזה נמרצת.
נהפוך הוא, בפתרון מימי מדולל הם יונים מתואמים [אל (H2O)6]+3 ואת הכלוריד. מבנים אלה דומים מאוד לאלה של diborane.
בדרך זו יש לך את הנוסחה אל2Cl6
אם ההבדל בין electronegativity של האטומים המרכיבים את הקשרים במתחם זה נמדדת, להלן ניתן לראות:
עבור אלומיניום אל הערך של electronegativity הוא 1.61 C וזה של כלור הוא 3.16 ג ההבדל ב electronegativity הוא 1.55 C.
על פי הכללים של התיאוריה מחייב, עבור תרכובת להיות יונית זה חייב להיות הבדל electronegativity של האטומים המרכיבים את הקשר של ערך גדול או שווה ל 1.7 C.
במקרה של הקשר אל-קל, ההבדל electronegativity הוא 1.55 C, אשר נותן אלומיניום trichloride הסדר מליטה קוולנטית. ערך קל זה ניתן לייחס את הקשרים המתואמים קוולנטיים שהוצגו על ידי המולקולה.
מאפיינים
גופנית
מראה: לבן מוצק, לפעמים צהוב בשל זיהומים הנגרמת על ידי כלור Ferric
צפיפות: 2.48 גרם / מ"ל
מסה טוחנת: 133.34 גרם / mol
סובלימציה: סובלימטס ב 178 מעלות צלזיוס, כך נקודות ההתכה שלה רותחים נמוכים מאוד.
נהיגה: מנוהל בצורה גרועה.
מסיסות: זה לא מסיס במים כי זה חומצה לואיס. הוא מסיס ממיסים אורגניים כגון בנזן, פחמן tetrachloride ו chloroform.
כימיקלים
במים trichloride אלומיניום הוא הידרוליזה להרכיב HCl ואת יון הידרוניום ואת hydroxide אלומיניום:
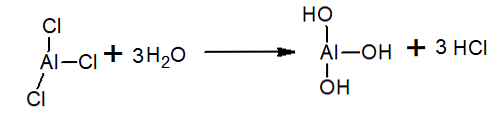
הוא משמש בתגובות פרידל-קרפט כזרז (חומר שניתן לשחזר בסוף התגובה, משום שהוא רק בו כדי להאיץ, להאט או ליזום תגובה).
זהו חומר קורוזיבי.
ב פירוק כאשר הוא מגיב באלימות עם מים זה מייצר תחמוצת אלומיניום גזים מסוכנים כגון מימן כלורי.
שימושים
- אנטיפרספיראנט.
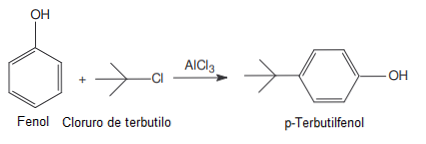
- Catalyst ב acylation ו alkylation של פרידל- Crafts.
סיכונים: השפעות אפשריות
- זהו חומר קורוזיבי, גורם לכוויות על העור ולנזק בעין חמורה.
- מגיב באלימות עם מים.
- זה מסוכן לסביבה.
- רעיל מאוד לאורגניזמים מימיים.
המלצות
הימנע מחשיפה למוצר ללא אמצעי הבטיחות הדרושים. חייבים להשתמש, משקפי מגן, כפפות, בגדים מתאימים, נעליים מכוסות.
במקרה של שאיפה. שאיפת אבק יכולה לגרות את מערכת הנשימה בשל אופיו המאכל של החומר. הסימפטומים כוללים כאב גרון, שיעול וקוצר נשימה. הסימפטומים של בצקת ריאות עשוי להיות מאוחר במקרים חמורים יכול להיות קטלני. להעביר את הקורבן למקום אוורירי ללא מזהמים. לספק הנשימה מלאכותית במידת הצורך. אם אתה מתקשה לנשום, לספק חמצן. התקשר לרופא.
במקרה של מגע עם העור. AlCl3 זה מאכל. זה יכול לגרום לגירוי או כוויות עם אדמומיות וכאב. לשטוף מיד לאחר מגע עם הרבה מים במשך 20 דקות לפחות. אין לנטרל או להוסיף חומרים שאינם מים. הסר בגדים מזוהמים ולשטוף אותו לפני שימוש חוזר. מיד להתייעץ עם הרופא במקרה של פגיעה.
במגע עם העיניים. AlCl3 זה מאכל. זה גורם לכאב עז, ראייה מטושטשת, נזק לרקמות. מיד לשטוף את העיניים עם מים במשך 20 דקות לפחות, ולשמור על העפעפיים פתוח כדי להבטיח את העין כולה ואת רקמות העפעפיים נמחקים. שטיפת העיניים תוך שניות היא חיונית להשגת יעילות מרבית. אם יש לך עדשות מגע, להסיר אותם לאחר 5 הדקות הראשונות ולאחר מכן להמשיך לשטוף את העיניים. התייעץ עם הרופא. זה יכול לגרום נזק רציני קרנית, הלחמית או חלקים אחרים של העין.
במקרה של בליעה. AlCl3 זה מאכל. שריפה יכולה לגרום לכאב בפה והוושט והכוויות של הריריות הריריות. זה יכול לייצר אי נוחות במערכת העיכול עם כאבי בטן, בחילה, הקאות ושלשולים. אל תתחיל להקיא. שוטפים את הפה, ולתת מים לשתות. לעולם אל תיתן שום דבר בעל פה לאדם לא מודע. התקשר לרופא. אם הקאות מתרחשות באופן ספונטני, הנח את הקורבן בצד שלו כדי להפחית את הסיכון לשאיפה.
אנשים עם הפרעות עור קיימות או בעיות עיניים או תפקוד נשימה לקוי עשויים להיות רגישים יותר להשפעות של החומר
אריזה ואחסנה של מתחם AlCl3 חייב להיעשות במקומות מאווררים, נקיים ויבשים.
הפניות
- ספר כימי, (2017), אלומיניום כלוריד. משוחזר מ
- cosmos מקוון, cosmos.com.mx
- Sharpe, A.G, (1993), כימיה אורגנית, ספרד, עריכה Reverté, S.A..
- F., (2017), AlCl אלומיניום כלוריד3, הסמלים. נלקח מblog.elinsignia.com.
- TriHealth, (2018), אלומיניום Trichloride, עדכון אחרון, 4 מרס, 2018, מתוך trihealth.adam.com.
- RxWiki, (s.f), אלומיניום כלוריד, מתוך, rxwiki.com.


