מאפייני טריפנוסומה brucei, מורפולוגיה, מחזור ביולוגי, סימפטומים
טריפנוסומה ברוסי זה טפיל תאיים פרוטוזהא. שייך בכיתה Kinetoplastidae, משפחה Trypanosomatidae סוג טריפנוסומה. ישנן שתי תת-מינים הגורמות לשתי גרסאות שונות של טריפנוסומיאזיס אנושיים או המכונה גם "מחלת שינה".
טריפנוסומה ברוסי תת. גמבינס, גורם לצורה הכרונית ו -98% מהמקרים, הממוקמים במערב אפריקה ומרכז אפריקה. טריפנוסומה ברוסי תת. רודזיה הוא הגורם של הצורה החריפה, נוכח במרכז וממזרח לאפריקה שמדרום לסהרה.
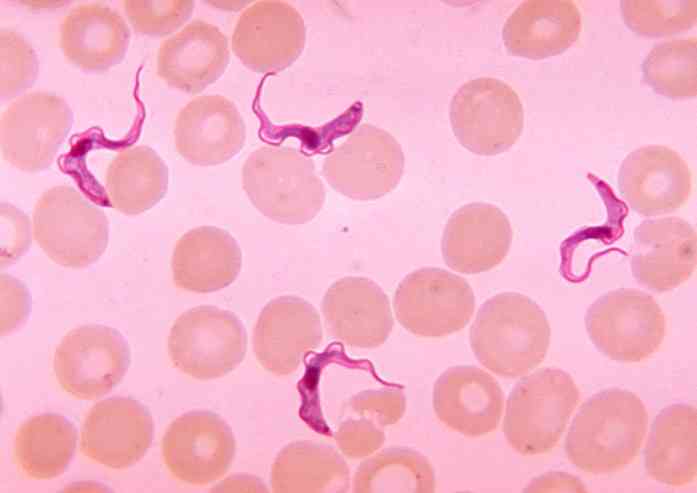
שני הווריאציות של מחלה זו דווחו באותן מדינות של אפריקה שמדרום לסהרה, שם נמצא הזנב tsetse, Glossina spp, וקטור או סוכן משדר של ט ברוסי.
תת-מימד שלישי, טריפנוסומה ברוסי תת. brucei, גורם למחלה דומה בבעלי חיים מקומיים ופראיים, הנקראים נאגאנה.
"מחלת השינה" מאיימת על יותר מ -60 מיליון בני אדם ב -36 מדינות באפריקה שמדרום לסהרה. ישנם כ -300,000 עד 500,000 מקרים בשנה, מתוכם כ-70,000 עד 100,000 מתים. ההתפשטות על ידי זבוב tsetse משתרע על שטח של 10 מיליון קילומטרים רבועים, שליש מהקרקע של אפריקה.
ארגון הבריאות העולמי מכיר בירידה משמעותית במספר המקרים החדשים של טריפנוסומיאזיס אנושיים בשנים האחרונות. זאת בשל ההתמדה של יוזמות לאומיות ובינלאומיות לשלוט במחלה זו.
אינדקס
- 1 מאפיינים כלליים
- 1.1 התגלית
- 1.2 גנטיקה
- 1.3 "מחלת השינה" והתחממות כדור הארץ
- 2 פילוגניות וטקסונומיה
- 3 מורפולוגיה
- 3.1 Tryomastigote טופס
- 3.2 טופס אפימסטיגוטה
- 3.3 הקינטוזום
- מחזור ביולוגי
- 4.1 ב המארח (אדם או יונקים אחרים)
- 4.2 ב זבוב tsetse (וקטור)
- 5 תסמינים של זיהום
- 5.1 שלב ראשון
- 5.2 שלב שני
- 5.3 אבחון
- 6 טיפול
- 7 הפניות
מאפיינים כלליים
זה נקרא "מחלת שינה" כי זה גורם היפוך מחזור השינה הטבעי של המטופל. האדם ישן במשך היום ונשאר ער בלילה. זהו תוצר של סדרה של הפרעות נפשיות ונוירולוגיות שהמחלה גורמת בשלב מתקדם.
התגלית
בעלי חיים או טריאגנוסומיאזיס היא מחלה חשובה בבקר באפריקה. הוא הזדהה טריפנוסומה ברוסי כמו סוכן סיבתי בשנת 1899. זה היה דוד ברוס תוך חקירת התפרצות גדולה של נאגאנה Zululand.
מאוחר יותר זיהה אלדו קסטלני מין זה של טריפנוסום בדם ובנוזל מוחי של חולים אנושיים עם "מחלת שינה".
בין השנים 1902 ו- 1910 זוהו שתי הגרסאות של המחלה בבני אדם ובתת-המין הסיבתי שלהם. הן חיות והן בני אדם יכולים לפעול כמאגרי טפילים המסוגלים לגרום למחלה בבני אדם.
גנטיקה
הגנום של גרעין טריפנוסומה ברוסי זה מורכב מ 11 כרומוזומים דיפלואידי ומאה microchromoses. בסך הכל יש 9,068 גנים. הגנום של המיטוכונדריה (הקינטופלסט) מורכב מניסויים רבים של דנ"א עגול.
"מחלת השינה" והתחממות כדור הארץ
טריפנוסומיאזיס אנושית אנושית נחשבת לאחת מתוך 12 מחלות זיהומיות אנושיות העלולות להחמיר עקב התחממות כדור הארץ.
זאת בשל העובדה שכאשר טמפרטורת הסביבה תגדל, האזור יהיה רגיש להיות כבוש על ידי זבוב יוגדל. Glossina sp. כאשר יתיישבו שטחים חדשים לטוס, זה ייקח את זה טפיל.
פילוגניות וטקסונומיה
Trypanosoma brucei pשייך לממלכה Protista, קבוצת Excavata, מחלת Euglenozoa, בכיתה Kinetoplastidae, סדר Trypanosomatida, משפחה Trypanosomatidae, סוג טריפנוסומה, משנה טריפנוזון.
למין זה יש שלוש תת-מינים הגורמות לגורמים שונים של "מחלת השינה" בבני אדם (ט. ב. תת. גמבינס ו ט. ב. תת. ייצורHodesian) ובחיות ביתיות ופראיות (ט. ב. תת. brucei).
מורפולוגיה
טופס Tripomastigote
טריפנוסומה ברוסי הוא אורגניזם תאיים מוארכים של 20 מיקרומטר ארוך 1-3 מיקרומטר רחב, אשר צורה, מבנה הרכב הממברנה להשתנות לאורך מחזור החיים שלה.
יש לו שתי צורות בסיסיות. צורה tripomastigote של הגוף הבסיסי האחורי לגרעין ו flagellum ארוך. צורה זו בתורו מניחה תת-סוגים במהלך מחזור החיים. מתוכם, תת סוג קצר או מעוקל (רפה באנגלית), הוא עבה יותר והגלגל שלו קצר.
טופס להבהיר
הצורה הבסיסית השנייה היא epimastigote של הגוף הקדמי הקדמי לגרעין ו flagellum קצת יותר קצר הקודם.
התא מכוסה על ידי שכבה של גליקופרוטין השטח משתנה. שכבה זו משנה את גליקופרוטאינים של פני השטח שלה ובכך חומק את ההתקפה של הנוגדנים שנוצרו על ידי המארח.
המערכת החיסונית מייצרת נוגדנים חדשים לתקוף את התצורה החדשה של השכבה ואת השכבה משתנה שוב. זה מה שנקרא וריאציה אנטיגנית.
הקינטוזומה
תכונה חשובה היא נוכחות של קינטוזומה. מבנה זה מורכב דנ"א מיטוכונדריאלי מרוכז הממוקם בתוך המיטוכונדריה היחידה הנוכחי. מיטוכונדריה גדולה זו ממוקמת בבסיס הנגע.
מחזור ביולוגי
מחזור החיים של טריפנוסומה ברוסי לסירוגין בין זבוב tsetse כמו וקטור לבין האדם כמארחת. כדי לפתח מארחים שונים כאלה, הפרוטוזון עובר שינויים מטבוליים ומורפולוגיים חשובים אחד למשנהו.
בזבוב, טריפנוסומה ברוסי מיושב בדרכי העיכול, בעוד שבאדם הוא נמצא בדם.
ב המארח (אדם או יונקים אחרים)
טריפנוסומה ברוסי זה מגיע בשלוש צורות בסיסיות לאורך כל מחזור שלה. כאשר הזבוב נושך אדם או יונק אחר כדי לחלץ את הדם שלו, הוא מזריק מהבלוטות הרוקיות אל תוך הדם צורה לא פולשנית של הפרוטוזואן, הקרויה מטאסיכיקלי.
פעם אחת בזרם הדם, היא הופכת לצורה השגשוגית, הנקראת דם רזה (רזה באנגלית).
צורת הדם הדקה טריפנוסומה ברוסי הוא מקבל את האנרגיה שלו מ glycolysis של גלוקוז הנוכחי בדם. תהליך מטבולי זה נעשה באורגנל הנקרא גליקוסומה. טריפנוזומים אלה מתרבים בנוזלי גוף שונים: דם, לימפה ונוזל שדרתי.
ככל שמספר הטפילים בדם עולה, הם מתחילים להשתנות שוב לצורה לא-פורצתנית. הפעם הוא גרסה עבה יותר עם דגלום קצר יותר, שנקרא דם שמנמן (מגושם).
את טריפנוסומים דם tuberous מותאמים לתנאי מערכת העיכול של הזבוב. הם מפעילים את המיטוכונדריה שלהם ואת האנזימים הדרושים למעגל חומצות הלימון ואת שרשרת הנשימה. מקור האנרגיה אינו עוד גלוקוז אלא פרולין.
בטס-טסה (הווקטור)
וקטור או סוכן משדר של טריפנוסומה ברוסי זה טס-טסה, Glossina spp. זה סוג המין 25 עד 30 מינים של זבובים hematophagous. הם קל להבדיל מן לטוס משותף על ידי חוטם ארוך במיוחד שלהם כנפיים מקופל במלואו במנוחה.
כאשר זבוב tsetse נושך את יונק המארח נגוע מחלץ את הדם, אלה צורות דם stubby לחדור את וקטור.
ברגע בדרכי העיכול של הזבוב, צורות דם קצרות הופכות במהירות לטריפנוזומים מתרבים פרוביפטיביים.
הם מתרבים על ידי ביקוע בינארי. הם עוזבים את מערכת העיכול של הזבוב ויוצאים לבלוטות הרוק. הם הופכים epimastigotes מעוגנים על הקירות על ידי הנגע.
בבלוטת הרוק, הם מתרבים והופכים לטריפנוסומים מטאסייקליים, מוכנים לחדור שוב למערכת הדם של יונק.
תסמינים של זיהום
תקופת הדגירה של המחלה היא 2 עד 3 ימים לאחר לנשוך את הזבוב. תסמינים נוירולוגיים עשויים להתרחש לאחר מספר חודשים במקרה של T. ב. תת. גמבינס. אם זה בערך ט. ב. תת. רודזיה, זה עלול לקחת שנים להתבטא.
השלב הראשון
ל"חולי השינה "יש שני שלבים. הראשון נקרא בשלב מוקדם או שלב hemolymphatic, הוא מאופיין על ידי נוכחות של טריפנוסומה ברוסי רק בדם ובלימפה.
במקרה זה, הסימפטומים הם חום, כאבי ראש, כאבי שרירים, הקאות, בלוטות לימפה נפוחות, ירידה במשקל, חולשה ועצבנות.
בשלב זה המחלה יכולה להתבלבל עם מלריה.
שלב שני
השלב שנקרא שלב מאוחר או שלב נוירולוגי (מצב אננצפליטי), מופעל עם הגעתו של הטפיל במערכת העצבים המרכזית, להיות מזוהה בנוזל cerebro-spinal. כאן הסימפטומים באים לידי ביטוי כשינויים בהתנהגות, בלבול, incoordination, שינוי מחזור השינה ולבסוף תרדמת.
התפתחות המחלה נמשכת במחזור של עד שלוש שנים במקרה של תת-מינים גמבינס, מסתיים במוות. כאשר תת-המין קיים רודזיה, המוות בא מחודשים עד חודשים.
מבין המקרים שאינם נתונים לטיפול, 100% מתים. 2-8% מהמקרים המטופלים מתים גם הם.
אבחון
השלב האבחוני הוא כאשר הטופס זיהומיות, כלומר טריפנוסום הדם, נמצא בדם.
באמצעות בדיקה מיקרוסקופית של דגימות דם, הצורה הספציפית של הטפיל מזוהה. בשלב האנצפליטי נדרש ניקור מותני כדי לנתח את הנוזל השדרתי.
ישנן מספר טכניקות מולקולריות כדי לאבחן את הנוכחות של טריפנוסומה ברוסי.
טיפול
היכולת שיש לו טריפנוסומה ברוסי של שינוי מתמיד של התצורה של השכבה החיצונית של גליקופרוטאינים (וריאציה אנטיגנית), מקשה מאוד על פיתוח חיסונים נגד "מחלת שינה".
אין כימותרפיה מניעתית וסיכוי קטן או חסר סיכוי לחיסון. ארבעת התרופות העיקריות המשמשות טריפנוסומיאזיס אפריקאיות אנושיות הן רעילות.
Melarsoprol הוא התרופה היחידה כי הוא יעיל עבור שני גרסאות של מערכת העצבים המרכזית. עם זאת, הוא כל כך רעיל כי הוא הורג 5% מהחולים המקבלים את זה.
Eflornithine, לבד או בשילוב עם nifurtimox, משמש יותר ויותר בתור השורה הראשונה של הטיפול במחלה הנגרמת על ידי טריפנוסומה ברוסי תת. גמבינס.
הפניות
- פן K ו KR מתיוס (2007) הביולוגיה של התא של טריפנוסומה brucei בידול. הדעה הנוכחית במיקרוביולוגיה. 10: 539-546.
- Fernández-Moya SM (2013) אפיון פונקציונלי של חלבונים RNA מחייב RBP33 ו DRBD3 כמו הרגולטורים של ביטוי גנים של טריפנוסומה ברוסי. דוקטורלית. המכון לפרזיטולוגיה וביו-רפואה "לופז-נירה". עריכה אוניברסיטת גרנדה, ספרד. 189 עמ '.
- García-Salcedo JA, D Pérez-Morga, P Gijón, V Dilbeck, E Pays ו- DP Nolan (2004) תפקיד דיפרנציאלי לאקטין במהלך מחזור החיים של Trypanosoma brucei. כתב העת EMBO 23: 780-789.
- קנדי PGE (2008) הבעיה המתמשכת של טריפנוסומיאזיס אפריקאי אנושי (מחלת השינה). תולדות נוירולוגיה, 64 (2), 116-126.
- מתיוס KR (2005) ביולוגיה התא ההתפתחותי של טריפנוסומה ברוסי. J. Cell Sci 118: 283-290.
- Welburn SC, EM Fèvre, PG קולמן, M Odiit ו- I Maudlin (2001) מחלת השינה: סיפור של שתי מחלות. טרדות בטפיל. 17 (1): 19-24.


